 Calvinzyklus
CalvinzyklusIm Calvinzyklus (oder auch Dunkelreaktion genannt) werden dann die Elektronen die im NADPH vorliegen und die Energie aus dem ATP genutzt, um energiearmes CO
2 zu binden und daraus energiereichen Zucker (Glucose) zu synthetisieren. Dieser Zucker ist der Ausgangspunkt für den weiteren Energiefluss in allen Lebewesen.
Das Binden von Energie und Kohlenstoff wird in der Ökologie
auch als Primärproduktion bezeichnet und die Organismen, die sie durchführen
als Primärproduzenten. Die Lebewesen, die Primärproduzenten fressen, nennt man
Primärkonsumenten, sie sind Teile einer Nahrungskette in der Energie und
Nährstoffe zwischen den Organismen weitergegeben werden. Konsumenten wandeln
die chemisch gebundene Energie aus den Primärproduzenten wieder in ATP um, das
sie beispielsweise in den Muskeln nutzen um sich fortzubewegen.
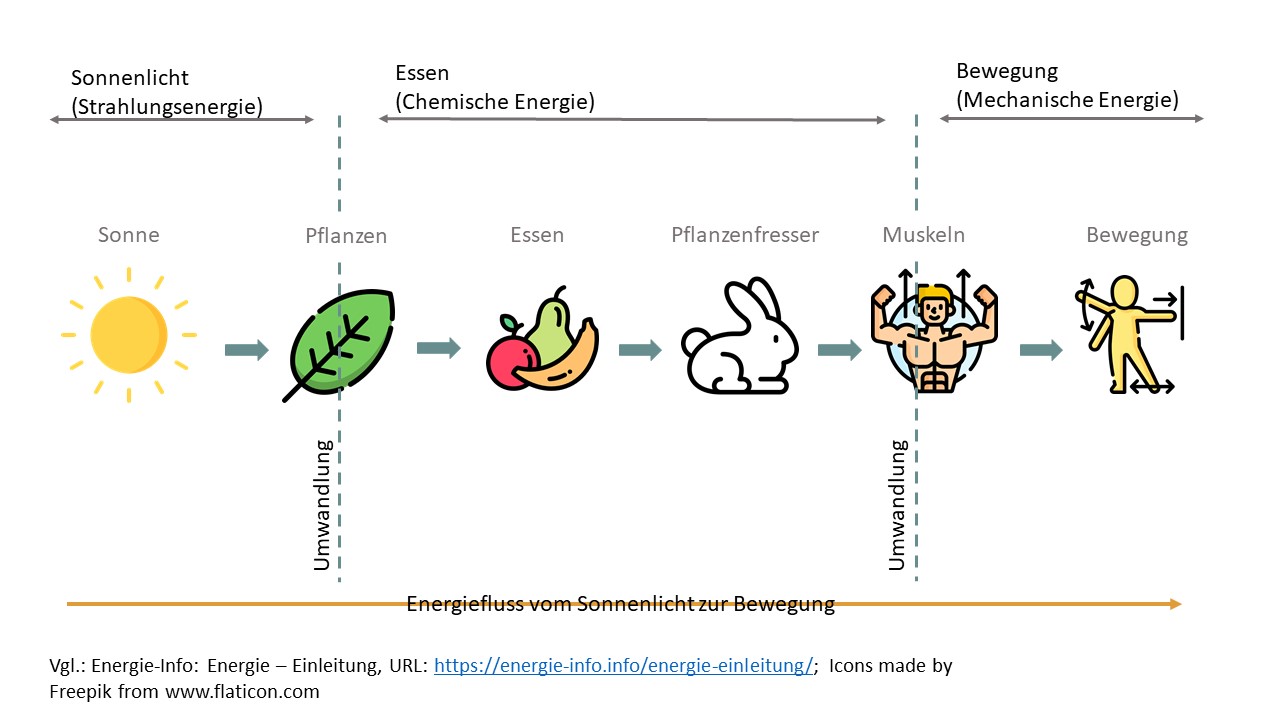
Die verschiedenen Konsumenten führen einen Prozess durch der
als Gegenstück zur Photosynthese gilt, die aerobe Atmung. Dabei wird die
Glucose schrittweise zu CO2 abgebaut, dabei werden Elektronen frei die über
eine Elektronentransportkette auf Sauerstoff übertragen werden, wobei Wasser
entsteht. Der Sauerstoff wird hierbei auch als terminaler Elektronenakzeptor
bezeichnet. Der Elektronenfluss wird wieder genutzt um einen Protonengradient
aufzubauen. Dieser Protonengradient wird wie bei der Photosynthese genutzt um
mit der ATPase ATP zu generieren. In den Lebewesen finden also viele
Umwandlungen von chemischer Energie in andere Formen chemischer Energie statt.
Die Umwandlung ist dabei nie vollständig, bei jeder Umwandlung wird auch Wärme
freigesetzt.
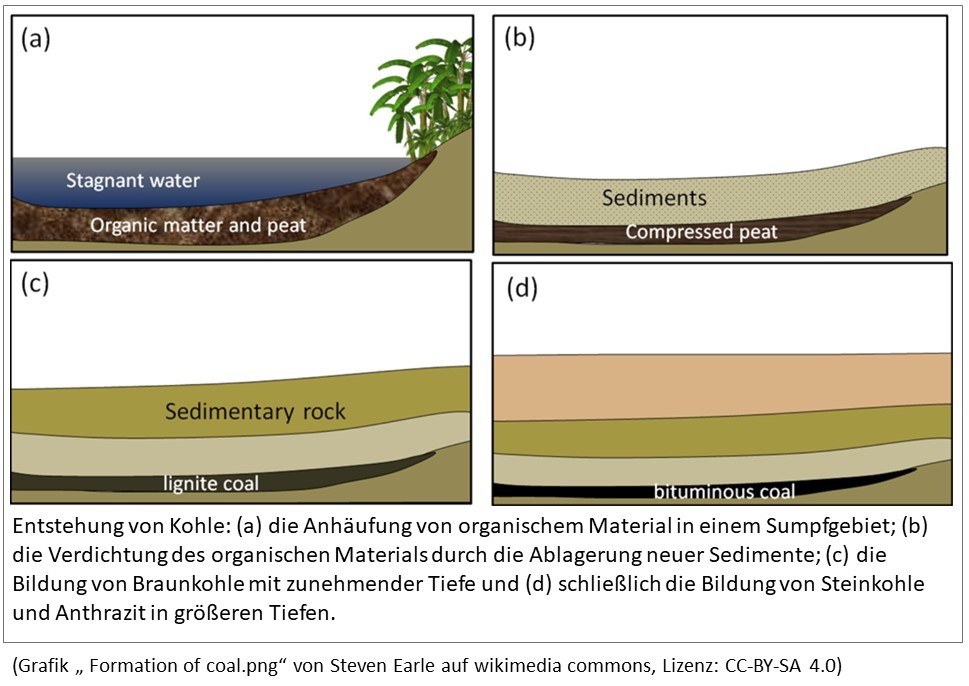 In der Vergangenheit kam es vor, dass große Mengen Biomasse
auf der Erdoberfläche abstarben und nicht zu CO2 zersetzt wurden. Diese wurden
durch einen Prozess, der als Inkohlung bezeichnet wird, zu den heutigen
fossilen Energieträgern. Zuerst entstand Torf, der auch heute unter Mooren
gefunden wird und unter sauerstoffarmen und nährstoffarmen Bedingungen an mit
Wasser überschichteten Orten entsteht. Über lange Zeiträume wird der durch
Ablagerungen und Wasser bedeckt, dabei wirken Druck und erhöhte Temperaturen
auf das organische Material, welches komprimiert und sich chemisch verändert.
Gase und Wasser werden abgeschieden. Über Millionen von Jahren bildeten sich
aus dieser Biomasse, die chemische Energie enthält, dann Kohle, Erdöl und
Erdgas. Wobei Kohle durch das Absterben von Wäldern an Land und Erdöl und
Erdgas durch das Absterben von Phytoplankton (Algen und Bakterien, die
Photsynthese betreiben) in Meeren entstanden.
In der Vergangenheit kam es vor, dass große Mengen Biomasse
auf der Erdoberfläche abstarben und nicht zu CO2 zersetzt wurden. Diese wurden
durch einen Prozess, der als Inkohlung bezeichnet wird, zu den heutigen
fossilen Energieträgern. Zuerst entstand Torf, der auch heute unter Mooren
gefunden wird und unter sauerstoffarmen und nährstoffarmen Bedingungen an mit
Wasser überschichteten Orten entsteht. Über lange Zeiträume wird der durch
Ablagerungen und Wasser bedeckt, dabei wirken Druck und erhöhte Temperaturen
auf das organische Material, welches komprimiert und sich chemisch verändert.
Gase und Wasser werden abgeschieden. Über Millionen von Jahren bildeten sich
aus dieser Biomasse, die chemische Energie enthält, dann Kohle, Erdöl und
Erdgas. Wobei Kohle durch das Absterben von Wäldern an Land und Erdöl und
Erdgas durch das Absterben von Phytoplankton (Algen und Bakterien, die
Photsynthese betreiben) in Meeren entstanden.